-
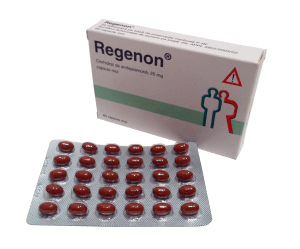
EMA建议撤销苯丙胺酮药物的上市许可
EMA的安全委员会(PRAC)建议撤销安非拉酮肥胖药物的欧盟营销授权。该建议是在一项审查之后提出的,该审查发现,出于安全原因限制使用这些药物的措施不够有效。它发现这些药物的使用时间超过推荐的最长期限3个月,从而可能增加严重副作用的风险,如肺动脉高血压和依赖性。这些药物也用于有心脏病或精神疾病史的患者,增加了他们患心脏病和精神问题的风险。此外,有证据表明在怀孕期间使用,这可能会对未出生的婴儿构成风险。该评价考虑了与这些问题有关的所有现有信息,包括来自德国和丹麦使用安非拉酮药物的两项研究的数据。此外
2022-06-11 -
EMA 建议在欧盟 (EU) 授予 Xenpozyme(寡肽酶 α)的上市许可
EMA 建议在欧盟 (EU) 授予 Xenpozyme(寡肽酶 α)的上市许可,这是一种治疗酸性鞘磷脂酶缺乏症 (ASMD) 的非中枢神经系统 (CNS) 表现的疗法,这是一种罕见的进行性遗传病。Xenpozyme适用于所有年龄段的A / B型或B型ASMD的儿童和成人。历史上被称为Niemann-Pick病A型(NPD A)和B(NPD B),ASMD是一种遗传性疾病。它属于称为“溶酶体贮积病”的代谢紊乱的更大家族,其中脂肪积聚在分解营养物质和其他物质的身体细胞部分。这会影响细胞的工作方式并导
2022-05-21 -

FDA批准嗜酸性粒细胞性食管炎的首个疗法
今天,美国食品和药物管理局批准 Dupixent (dupilumab) 用于治疗体重至少 40 公斤(约 88 磅)的 12 岁及以上成人和儿童患者的嗜酸性食管炎 (EoE)。今天的行动标志着 FDA 首次批准 EoE 治疗。“近年来,随着研究人员和临床医生对嗜酸粒细胞性食管炎的了解越来越多,美国发现和诊断出更多的病例,”FDA 药物评估和药物评估中心胃肠病学部主任 Jessica Lee 医学博士说。研究。“今天的批准将满足越来越多的嗜酸性食管炎患者的重要未满足需求。”EoE 是一种慢性炎症
2022-05-21 -
FDA将辉瑞BioNTech COVID-19疫苗加强剂量的资格扩大到5至11岁的儿童
今天,美国食品和药物管理局修改了辉瑞生物技术公司(Pfizer BioNTech)2019冠状病毒疾病疫苗的紧急使用授权(EUA),授权在完成辉瑞生物技术公司(Pfizer BioNTech)2019冠状病毒疾病疫苗的主要系列后至少五个月,对5岁至11岁的个体使用单一增强剂量。FDA专员Robert M.Califf说:“虽然2019冠状病毒疾病在儿童中的严重程度通常比成人轻,但omicron波已经看到更多的儿童患病并住院,儿童也可能经历长期影响,即使最初是轻度疾病。”,医学博士。“美国食品和药
2022-05-21 -
默沙东莫诺匹韦 (molnupiravir)获FDA紧急使用授权 (EUA)
12月23日,美国食品药品监督管理局( FDA )为默克( Merck )公司的莫诺匹韦 (molnupiravir )颁发了紧急使用授权 (EUA),用于治疗 SARS-CoV-2 病毒直接检测结果呈阳性的成人轻中度冠状病毒病 (COVID-19),并且有发展为严重 COVID-19 的高风险,包括住院或死亡,以及 FDA 授权的 COVID-19 替代治疗方案无法获得或临床上不合适的人。Molnupiravir 仅可通过处方获得,应在诊断出 COVID-19 后并在症状出现后五天内尽快开始使
2021-12-24 -
EMA 推荐 Nuvaxovid 在欧盟获得授权
更新: Nuvaxovid 现在已在整个欧盟获得授权。在此之前,欧盟委员会于 2021 年 12 月 20 日授予了有条件的 营销授权。 EMA 建议授予Novavax 的 COVID-19疫苗 Nuvaxovid(也称为 NVX-CoV2373)有条件的营销授权,以预防 18 岁以上人群发生 COVID-19。 Nuvaxovid 是欧盟推荐的第五种预防 COVID-19 的疫苗。它是一种基于蛋白质的疫苗,与已经获得批准的疫苗一起,将在大流行的关键阶段支持欧盟成员国的疫苗接
2021-12-21 -
FDA 批准首个用于 HIV 暴露前预防的注射治疗
2021年12月20日,美国食品和药物管理局批准 Apreude(cabotegravir 缓释注射悬浮液)用于体重至少 35 公斤(77 磅)的高危成人和青少年进行暴露前预防(PrEP),以降低性行为风险获得艾滋病毒。Apreude 首先作为间隔一个月的两次初始注射给药,然后每两个月给药一次。患者可以开始使用 Apreude 进行治疗,也可以口服 cabotegravir (Vocabria) 四个星期,以评估他们对该药物的耐受程度。 “今天的批准为结束 HIV 流行的努力增加了一个
2021-12-21 -

FDA 批准治疗重症肌无力的新疗法Vyvgart(efgartigimod)
2021年12月17日,美国食品和药物管理局批准了 Vyvgart(efgartigimod)用于治疗抗乙酰胆碱受体(AChR)抗体检测呈阳性的成人全身性重症肌无力(gMG)。 该批准是针对这种罕见的慢性自身免疫性神经肌肉疾病的新一类药物的首个批准。重症肌无力是一种慢性自身免疫性神经肌肉疾病,导致骨骼肌(也称为随意肌)虚弱,在活动期后恶化并在休息期后好转。重症肌无力会影响随意肌,尤其是那些负责控制眼睛、面部、嘴巴、喉咙和四肢的肌肉。在重症肌无力中,免疫系统会产生 AChR 抗体,干扰神
2021-12-19 -
EMA 建议在欧盟授予Oxbryta(voxelotor)的上市许可(镰状细胞病的新疗法)
EMA 建议在欧盟授予Oxbryta(voxelotor)的上市许可,用于治疗 12 岁及以上患者的镰状细胞病引起的溶血性贫血(红细胞过度分解)。Oxbryta 可单独使用或与hydroxycarbamide (羟基脲,也称为hydroxyurea)组合使用。镰状细胞病是一种遗传病,其中红细胞变得僵硬和粘稠,并从圆盘形变为新月形(如镰刀)。形状的变化是由异常形式的血红蛋白(红细胞中携带氧气到全身各处的蛋白质)的存在引起的。在镰状细胞性贫血患者中,异常的镰状红细胞阻塞血管,限制血液流向器官,如心脏
2021-12-19 -

EMA 发布关于使用 Paxlovid(PF-07321332 和利托那韦)治疗 COVID-19 的建议
EMA 的人用药物委员会 ( CHMP ) 已发布关于使用 Paxlovid(PF-07321332 和利托那韦)治疗 COVID-19 的建议。该药物尚未在欧盟获得授权,可用于治疗不需要补充氧气且进展为严重疾病风险增加的 COVID-19 成人。应在诊断出 COVID-19 后尽快并在出现症状后 5 天内使用 Paxlovid。该药物的两种活性物质PF-07321332 和利托那韦作为单独的片剂提供,应每天服用两次,连续服用 5 天。鉴于整个欧盟因 COVID-19 引起的感染率和死亡率上升,
2021-12-19 -
COVID-19:EMA 建议授权抗体药物 Xevudy
EMA 的人用药物委员会 ( CHMP ) 已建议授权单克隆抗体 Xevudy ( sotrovimab ) 用于治疗 COVID-19。申请人为葛兰素史克贸易服务有限公司,与 Vir Biotechnology共同开发该药物。委员会建议授权 Xevudy 用于治疗不需要补充氧气且疾病恶化风险增加的成人和青少年(12 岁以上,体重至少 40 公斤)的 COVID-19。 继11月Regkirona和Ronapreve获得批准之后,Xevudy 是欧盟推荐用于治疗 COVID-19 的第
2021-12-19 -
EMA 建议批准在重症 COVID-19 成人患者中使用 RoActemra
欧盟EMA的人用药物委员会(CHMP)建议扩大RoActemra(托珠单抗)的适应症,以包括正在接受皮质类固醇全身治疗并需要补充氧气或机械通气的COVID-19成人患者的治疗。该药物由罗氏公司销售,已在欧盟获得批准,用于治疗炎症性疾病类风湿性关节炎,全身性幼年特发性关节炎,幼年特发性多关节炎,巨细胞动脉炎和细胞因子释放综合征(CRS)。新冠肺炎疫情研究数据CHMP评估了一项主要研究的数据,该研究涉及4,116名患有严重COVID-19的住院成年人,他们需要额外的氧气或机械通气,并且血液中含有高水
2021-12-07 -
FDA将两种用于治疗和暴露后预防COVID-19的单克隆抗体的授权范围扩大到包括新生儿在内的年轻儿科患者
今天,美国食品和药物管理局修订了巴姆拉尼单抗(bamlanivimab)和依替昔单抗(etesevimab)(已被授权用于体重至少40公斤或约88磅的12岁及以上儿科患者)的紧急使用授权(EUA),额外授权巴姆尼尼单抗和依替昔单抗一起用于治疗所有年轻儿科患者的轻度至中度COVID-19, 包括COVID-19检测呈阳性且进展为严重COVID-19(包括住院或死亡)的高风险新生儿。该修订还授权巴姆拉尼单抗和依替昔维单抗一起给药,用于所有进展为严重COVID-19(包括住院或死亡)高风险的儿科患者(
2021-12-04 -

FDA 批准新的成像药物Cytalux(pafolacianine)以帮助识别卵巢癌病变
美国食品和药物管理局今天批准了 Cytalux(pafolacianine),这是一种成像药物,旨在帮助外科医生识别卵巢癌病变。该药物旨在提高定位通常在手术过程中难以检测到的额外卵巢癌组织的能力。Cytalux 适用于成年卵巢癌患者,以帮助识别手术过程中的癌性病变。该药物是一种诊断剂,在手术前以静脉注射的形式给药。“FDA 对 Cytalux 的批准有助于提高外科医生识别可能无法检测到的致命卵巢肿瘤的能力,”FDA 药物评价和研究中心专业医学办公室副主任 Alex Gorovets 医学博士说,
2021-11-30 -
EMA 建议批准Comirnaty COVID-19 疫苗用于 5 至 11 岁儿童
EMA的人用药物委员会(CHMP)建议扩大COVID-19疫苗Comirnaty的适应症,使其可用于5至11岁的儿童。该疫苗由BioNTech和辉瑞公司开发,已被批准用于成人和12岁及以上的儿童。在 5 至 11 岁的儿童中,Comirnaty 的剂量将低于 12 岁及以上人群使用的剂量(从30 µg降低为10 µg )。与更大年龄组一样,间隔三周在上臂肌肉中进行两次注射。 一项针对 5 至 11 岁儿童的主要研究表明,在该年龄组中以较低剂量 (10 µg) 给予 Comirnaty
2021-11-25 -
FDA批准对其他药物耐药的常见移植后感染的首个治疗方法
11月23日,美国FDA批准 Livtencity(maribavir)作为第一种治疗移植后巨细胞病毒 (CMV) 感染,用于对可用的 CMV 抗病毒治疗没有反应(有或没有导致抗性的基因突变)的成人和儿童患者(12 岁及以上,体重至少 35 公斤)。Livtencity 通过阻止人类巨细胞病毒酶 pUL97 的活性起作用,从而阻止病毒复制。“当面临巨细胞病毒感染时,移植接受者面临更大的并发症和死亡风险,”FDA 药物评价和研究中心传染病办公室主任、医学博士、公共卫生硕士 John Farley
2021-11-24

